#desmielinizantes #esclerosemúltipla #EM #NMO #antiMOG
Bem-vindo ou bem-vinda a mais um skycast premium!
Aqui quem fala é Mariana Dalaqua, Neurorradiologista, e estou aqui para resumir pra você um artigo publicado em junho de 2019 na revista Brain, produzido após uma conferência realizada em Milão em 2018, escrito colaborativamente por experts em esclerose múltipla da Itália, Estados Unidos, Holanda, Reino Unido, Alemanha, Canadá e França.
O objetivo do artigo foi padronizar os achados de imagem por ressonância magnética (RM) para a correta interpretação e categorização das lesões que definem o diagnóstico de esclerose múltipla (EM). Foram estabelecidas quais são as lesões típicas, atípicas e quais não devem ser consideradas para o diagnóstico desta doença, sugestivas de diagnósticos alternativos. Adicionalmente, o artigo menciona alguns achados qualitativos emergentes das lesões, que provavelmente poderão fazer parte dos critérios diagnósticos no futuro.
Algumas outras doenças podem satisfazer os critérios radiológicos para EM, o que torna o diagnóstico desta doença mais desafiador, especialmente quando os biomarcadores laboratoriais não são conclusivos. A evolução técnica da RM contribuiu para definir melhor as localizações típicas da EM, bem como para a identificação de características mais específicas das lesões típicas (tais como o sinal da veia central, áreas de desmielinização subpial e as bordas das lesões).
Introdução
Desde sua introdução em 2001 até sua recente revisão em 2017, os critérios diagnósticos de McDonald baseiam-se no número, tamanho e localização das lesões encefálicas e medulares supostamente de aspecto típico para EM. A avaliação de lesões em hipersinal T2/FLAIR e com realce pelo contraste em T1 permitiu a definição de critérios que propiciam o diagnóstico precoce da doença em pacientes com sintomas característicos. A requisição de critérios de disseminação no tempo e no espaço permitem que tais critérios diagnósticos sejam altamente sensíveis no contexto de um evento desmielinizante (neurite óptica subaguda, mielite transversa incompleta, síndromes do tronco encefálico), com alto poder preditivo positivo para a distinção entre as formas recorrentes precoces das síndromes clínicas monofásicas isoladas, na exclusão de diagnósticos alternativos por avaliação clínica e laboratorial (testes sanguíneos, liquóricos, radiológicos e neurofisiológicos).
Considerações gerais para o uso da RM para o diagnóstico da EM
(Critérios diagnósticos de McDonald, 2017)
- A síndrome clínica deve ser típica de desmielinização;
- Os critérios devem ser aplicados para pacientes adultos (entre 18 e 50 anos), embora tenham boa acurácia em distinguir crianças com EM daquelas com episódios desmielinizantes monofásicos. Em crianças, a presença de pelo menos um “black hole” (lesão em hipossinal T1) e de pelo menos uma lesão periventricular contribui para esta diferenciação;
- Em pacientes de mais de 50 anos com fatores de risco cardiovasculares, critérios mais estritos devem ser considerados (ex: maior número de lesões periventriculares);
- O exame de RM deve ser de qualidade adequada, com poucos artefatos e realizado em campo magnético de pelo menos 1.5 Tesla. Devem ser adquiridas sequências que sejam volumétricas (3D) ou 2D com pelo menos 3 mm de espessura e sem espaço entre as fatias (protocolo sugerido na Tabela 1);
- Sequências-chave da RM incluem imagens do encéfalo e da medula espinhal ponderadas em T2 e em T1 antes e após o contraste;
- Lesões da EM podem ocorrer em qualquer lugar do sistema nervoso central (SNC), portanto a medula espinhal deve ser avaliada nos níveis cervical, torácico e lombar nos pacientes com sintomas correspondentes a estas localizações, e também para a detecção de lesões subclínicas. Inclusive, a avaliação medular é útil para estabelecer a disseminação no espaço quando o exame do encéfalo não é conclusivo e para fornecer informações prognósticas importantes;
- Sequências com supressão de gordura são importantes para a avaliação dos nervos ópticos, devendo ser consideradas especialmente em casos atípicos para excluir diagnósticos alternativos;
- A presença das lesões deve ser considerada em múltiplos planos, para evitar falsos positivos devido a artefatos, bem como falsos negativos. A aquisição de sequências 3D (ex: 3DT2-FLAIR) permite reconstruções multiplanares, enquanto se houver uma sequência original 2D, uma segunda sequência 2D deve ser adquirida em plano diferente;
- Imagens seriadas ajudam a fechar o diagnóstico de EM, pois os achados da doença tipicamente evoluem no tempo e no espaço;
- A interpretação dos exames de RM deve ser feita por (neuror)radiologistas treinados ou clínicos profundamente familiarizados com as características de imagem da doença e seus diagnósticos diferenciais;
- Lesões com hipersinal T2 podem aumentar, diminuir ou estabilizar ao longo do tempo. Mais raramente, lesões pequenas podem desaparecer completamente;
- O padrão de realce pelo gadolínio (Gd) nas lesões da EM é variável, porém quase sempre transitório (durando de 2 a 8 semanas, tipicamente menos que 4 semanas);
- Para o diagnóstico de EM, deve haver ao menos uma lesão típica em pelo menos duas regiões características (periventricular, cortico-justacortical, infratentorial, medular), para caracterizar a disseminação no espaço;
- Lesões da substância branca (SB) são comuns em pacientes com comorbidades vasculares ou enxaqueca, bem como em adultos saudáveis. Lesões pequenas, inespecíficas e arredondadas na SB profunda, poupando a zona periventricular e as fibras em “U”, também podem contribuir para os achados da RM. Atualmente, é difícil distinguir se lesões individuais são atribuíveis a desmielinização ou a comorbidades;
- Especialmente nos pacientes que têm poucas lesões, as características de cada lesão (tamanho, forma, orientação perpendicular ao ventrículo, hipointensidade em T1, padrão de realce, etc) são importantes para determinar se são típicas de EM ou não. Para pacientes com muitas lesões, a sua distribuição é mais relevante.
Tabela 1: Sequências de RM sugeridas para cada tipo de lesão | ||
Tipo de lesão | Sequência chave para a identificação | Sequências alternativas para confirmação diagnóstica |
Lesões típicas para os critérios diagnósticos | ||
Periventriculares | T2-FLAIR (pref. 3D) | T2-WI, PD-WI, 3DT1-MPRAGE |
Cortico-justacorticais | T2-FLAIR (pref. 3D) (lesões corticais: DIR) | 3DT1-MPRAGE, T2-WI, DIR, PSIR (lesões corticais: 3DT1-MPRAGE e PSIR; o T2-FLAIR não é tão bom) |
Infratentoriais | T2-FLAIR (pref. 3D) | T2-WI, PD-WI, 3DT1-MPRAGE |
Medulares (cervicais + torácicas) | ≥ 2 seq. sagitais incluindo STIR, T2-WI, PD-WI, PSIR ou 3DT1-MPRAGE | T2 axial |
Lesões com realce pelo Gd | T1-SE ou T1-GRE pós-Gd após ≥ 5 min da injeção | T1 pré-contraste (opcional) |
Lesões adicionais atualmente não incluídas nos critérios diagnósticos formais | ||
Nervos ópticos | 2D-STIR coronal T1-Gd fat sat axial e coronal | 2D-FSE coronal, 2D-STIR axial Seq. alternativas (menor resolução): 3D-DIR, 2D/3DT2-FSE, 2D/3DT2-FLAIR fat sat |
Achados baseados em características patofisiológicas (uso futuro) | ||
Sinal da veia central | 3DT2* T2-FLAIR* | SWI |
Desmielinização subpial | 7T-T2* ou MP2RAGE | PSIR e/ou 3DT1-MPRAGE; T2-FLAIR pior; DIR |
Lesões lentamente progressivas | 7T-T2*-GRE (fase) | 3T-3D-T2* (fase) ou SWI T1 ou T2 longitudinais |
DIR = double inversion recovery; EPI = echo-planar imaging; FSE = fast spin echo; GE = gradient echo; GRE = gradient recalled echo; MPRAGE = magnetization-prepared rapid gradient echo; MT = magnetization transfer; PD = proton density; PSIR = phase-sensitive inversion recovery; SE = spin echo; STIR = short-tau inversion recovery; SWI = susceptibility-weighted imaging; T2-FLAIR = T2-fluid-attenuated inversion recovery. | ||
Definição de lesões da esclerose múltipla
As lesões são definidas como áreas focais de hipersinal T2/FLAIR ou PD-WI, tipicamente arredondadas ou ovoides, variando de poucos milímetros a mais que 2 cm, visíveis em pelo menos duas imagens consecutivas (embora em exames de espessura ≥ 3 mm, as lesões possam ser eventualmente observadas em apenas uma imagem). Geralmente, precisam ter ao menos 3 mm no maior eixo para satisfazerem os critérios diagnósticos, embora a topografia também deva ser considerada (ex: lesão < 3 mm no assoalho do IV ventrículo deve ser considerada anormal).
As lesões da EM estão tipicamente presentes em ambos os hemisférios cerebrais, porém sua distribuição é geralmente assimétrica nos estágios precoces, podendo ocorrer em qualquer parte do SNC, embora atinjam preferencialmente as regiões-chave (periventricular, cortico-justacortical, corpo caloso, fossa posterior, medula espinhal – especialmente no segmento cervical). A avaliação destas áreas para caracterizar disseminação no espaço será discutida a seguir.
Lesões periventriculares (Figura 1)
- Definição: lesão em hipersinal T2/FLAIR na substância branca em contato direto com os ventrículos laterais. Lesões do corpo caloso que tocam o ventrículo estão incluídas nesta definição.
- Exceção: lesão que encosta nos ventrículos laterais, mas está localizada na substância cinzenta (SC) profunda.
- Distribuição típica: perivenular (ao longo das veias medulares profundas) e perpendicular à superfície ependimária, sendo ovais no plano axial (“dedos de Dawson”).
- Armadilhas: lesões periventriculares são encontradas em outras doenças, tais como enxaqueca, microangiopatia, infartos lacunares, espectro da neuromielite óptica (NMO-SD) e síndrome anti-MOG. Nestas condições, as lesões geralmente não tocam os ventrículos, não são perpendiculares à superfície ependimária ou no corpo caloso. Lesões que tocam o III ou IV ventrículos ou lesões mesencefálicas que tocam o aqueduto cerebral não devem ser contadas como periventriculares.
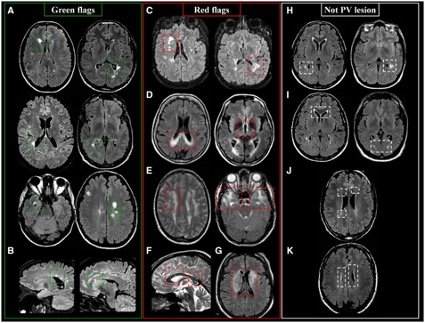
Figura 1 – Características das lesões periventriculares de esclerose múltipla que são típicas, atípicas e aquelas que não devem ser incluídas na contagem de lesões.
– Coluna da esquerda, lesões típicas: (A) exemplos de lesões periventriculares sugestivas de esclerose múltipla; (B) lesões periventriculares perpendiculares ao corpo caloso (“dedos de Dawson”).
– Coluna do meio, lesões atípicas: (C) lesões múltiplas da SB envolvendo regiões periventriculares e de SC profunda, sugestivas de doença isquêmica de pequenos vasos; (D) envolvimento extenso do corpo caloso posterior e lesões bilaterais diencefálicas em NMO-SD; (E) lesões múltiplas que afetam a SB profunda, cápsula externa e lobos temporais no CADASIL; (F) lesões intracalosas em “bola de neve” na síndrome de Susac; (G) lesões difusas e extensas que afetam tanto a SB quanto a SC profunda no lúpus eritematoso sistêmico.
PV = periventricular.
– Coluna da direita, lesões que não devem ser consideradas periventriculares: (H) lesão que não toca os ventrículos laterais; (I) ‘capping’ periventricular simétrico anterior e posterior; (J) lesão menor que 3 mm no eixo mais longo; (K) hiperintensidades lineares simétricas que encostam nos ventrículos laterais.
Lesões cortico-justacorticais (Figura 2)
- Definição e distribuição típica:
- lesão justacortical: lesão da SB em hipersinal T2/FLAIR em contato direto com o córtex. São mais evidentes em 3DT2-FLAIR e tipicamente envolvendo as fibras em “U”, localizadas em todos os lobos cerebrais e no cerebelo;
- lesão cortical: anormalidade focal completamente inserida no córtex ou abrangendo o córtex e a SB subjacente, que pode ser observada em 3DT2-FLAIR e ainda melhor em DIR (hipersinal em relação à SC normal adjacente, pelo menos 3 mm), PSIR ou T1-MPRAGE (em ambas, em hipossinal em relação ao córtex normal).
- Armadilhas: lesões próximas ao córtex podem estar presentes no envelhecimento normal e em outras doenças neurológicas (enxaqueca, microangiopatia), porém nestas condições costumam ser tipicamente na SB profunda e com uma faixa de SB as separando do córtex (à exceção de infartos corticais e vasculites). Fibras em “U” são tipicamente poupadas por hipóxia e doenças cerebrovasculares. Artefatos e veias podem simular lesões corticais especialmente nas sequências DIR e PSIR, devendo-se sempre verificar imagens consecutivas e a confirmar a presença das lesões em outras sequências.
- Observações: lesões corticais são uma característica distintiva da EM e facilitam a identificação de pacientes com síndromes clinicamente isoladas que correm maior risco de desenvolver um segundo episódio clínico. Não são encontradas em outras doenças que simulam EM, exceto em 3% dos pacientes com NMO-SD na fase aguda, tendendo a desaparecer nos exames de seguimento.
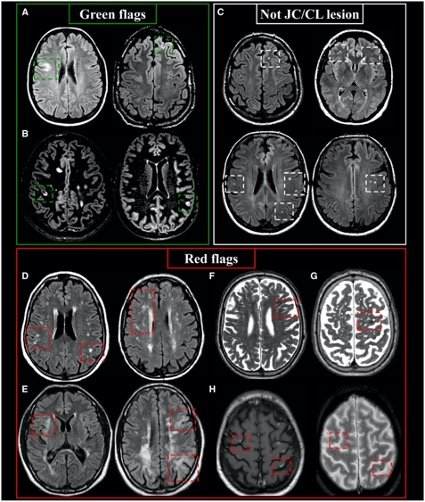
Figura 2 – Características da esclerose múltipla cortical/justacortical que são típicas, atípicas e que não devem ser incluídas.
– Em cima, à esquerda: exemplos de (A) lesões justacorticais e (B) lesões corticais sugestivas de esclerose múltipla.
– Em cima à direita: (C) lesões de SB que não tocam o córtex ou dentro do córtex (subcorticais).
– Linha inferior: (D) lesões múltiplas envolvendo a SB subcortical e profunda, sugestivas de doença de pequenos vasos; (E) lesões envolvendo a transição entre a SB-SC em diferentes lobos cerebrais, com margens mal definidas na leucoencefalopatia multifocal progressiva (LEMP); (F) múltiplas áreas alongadas e bem definidas em sinal do LCR, compatíveis com espaços perivasculares alargados; (G) hipointensidade focal em T2 compatível com hemossiderina (micro-hemorragia); (H) múltiplas áreas leptomeníngeas/corticais em hipersinal T1 e hipossinal em T2* em vasculite do SNC.
JC/CL = justacortical/cortical.
Lesões infratentoriais (Figura 3)
- Definição e distribuição típica: lesão em hipersinal T2/FLAIR em qualquer lugar do tronco encefálico, pedúnculos cerebelares ou cerebelo. Geralmente ocorrem perto da superfície (subpiais) ou, quando mais centrais, têm forma arredondada / ovoide (como ao longo do trato trigeminal), podendo ser únicas ou múltiplas / confluentes.
Na ponte, tipicamente envolvem o assoalho do IV ventrículo (tocando o fascículo longitudinal medial), a região subpial e os tratos trigeminais.
No mesencéfalo, tipicamente envolvem os pedúnculos cerebrais e estão próximas ao aqueduto cerebral.
No bulbo, podem ser paramedianas uni ou bilaterais.
- Armadilhas: Lesões pontinas lacunares isquêmicas também são frequentes, porém usualmente mais centrais e em zonas de fronteira vascular (ramos penetrantes da a. basilar e aa. cerebelares superiores). Envolvimento marcado dos pedúnculos cerebelares superiores e médios deve evocar síndrome anti-MOG e LEMP no diagnóstico diferencial, especialmente se as lesões forem de margens mal definidas. Lesões ao redor do aqueduto cerebral e na região dorsal do tronco encefálico, próximas ao IV ventrículo (na área postrema e trato solitário), são frequentes na NMO-SD, podendo determinar estenose aquedutal e hidrocefalia obstrutiva. Lesões diencefálicas e infratentoriais grandes devem evocar Neuro-Behçet no diagnóstico diferencial. Lesões típicas de CLIPPERS costumam ter padrão miliar.
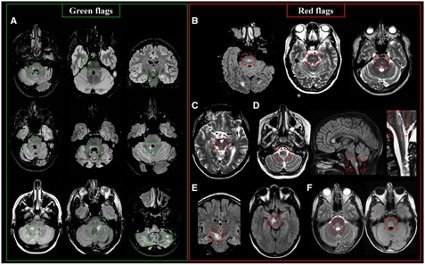
Figura 3 – Características das lesões de esclerose múltipla infratentoriais que são típicas e atípicas.
– Coluna da esquerda, lesões típicas: (A) exemplos de lesões infratentoriais sugestivas de esclerose múltipla.
– Coluna da direita, lesões atípicas: (B) lesões pontinas centrais e simétricas na microangiopatia; (C) lesão periaquedutal na NMO-SD; (D) lesões da área postrema na NMO-SD; (E) lesão mesencéfalo-diencefálica na síndrome anti-MOG; (F) grande lesão ovoide próxima ao assoalho do IV ventrículo na neuro-Behçet.
Lesões medulares (Figura 4)
- Definição e distribuição típica: lesões em hipersinal T2, tipicamente múltiplas, periféricas e curtas (extensão craniocaudal de menos de 2 corpos vertebrais e menos que metade da área transversa da medula), mais frequentes no segmento cervical. Devem ser identificadas em pelo menos duas sequências do exame ou em dois planos. Para serem consideradas típicas, devem ser focais e com margens bem definidas.
- Armadilhas: lesões estritamente restritas à SC são raras na EM. Lesões medulares não são observadas no envelhecimento normal ou na maioria das lesões neurovasculares. Lesões extensas no sentido craniocaudal (> 3 corpos vertebrais), com envolvimento preferencial da SC e edema marcado sugerem NMO-SD ou síndrome anti-MOG.
- Observações: lesões medulares ativas realçam com menos frequência que as lesões encefálicas ativas. Quando o realce está presente, desaparece rápido (2 a 8 semanas, tipicamente menos que 4 semanas) e é nodular. Realce anelar incompleto é incomum. As lesões podem ter efeito tumefativo na fase aguda.
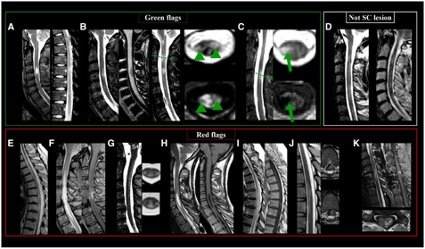
Figura 4 – Características das lesões medulares de esclerose múltipla que são típicas, atípicas e aquelas que não devem ser incluídas.
– Em cima, à esquerda: exemplos de (A) lesões medulares cervicais e torácicas em T2 sagital; (B) lesões medulares cervicais com hipossinal T1 em 3T (setas verdes); (C) uma lesão medular cervical com envolvimento da coluna lateral e SC central (setas verdes) em T2 e IR.
– Em cima, à direita: (D) lesões ‘difusas’ da medula espinhal com bordas mal definidas, não incluídas para a definição de envolvimento da medula espinhal.
– Linha inferior: (E) mielite transversa longitudinalmente extensa afetando mais de três segmentos vertebrais na NMO-SD; (F) lesão da medula espinhal longitudinalmente extensa afetando mais de três segmentos vertebrais associadas a realce leptomeníngeo e periférico na neurossarcoidose; (G) envolvimento extenso e seletivo das colunas laterais e posteriores na neurodegeneração combinada subaguda; (H) cavidades medulares na siringomielia; (I) extensa lesão com hipersinal T2, com regiões de realce heterogêneo pelo contraste em uma fístula arteriovenosa; (J) lesão anterior em hipersinal T2 na medula torácica, que se estende por mais de dois segmentos vertebrais em um caso de mielopatia isquêmica subaguda; (K) lesão em hipersinal T2 na medula cervical mostrando realce “tipo panqueca” em um caso de mielopatia espondilótica.
SC = medula espinhal.
Lesões com realce pelo Gd (Figura 5)
Pontos-chave:
- As preocupações com a segurança em relação à administração de gadolínio e sua tendência de se acumular no cérebro podem ser mitigadas pelo uso de agentes macrocíclicos em detrimento de agentes lineares, e pelo controle da frequência de administração do contraste nos exames de controle;
- Sua utilização auxilia a demonstrar a disseminação no tempo em um exame inicial, quando algumas lesões têm realce e outras não;
- Realce de lesões com atividade inflamatória costuma durar entre 2 e 8 semanas, tipicamente menos que 4 semanas. Lesões que realçam por mais de 3 meses são excepcionais na EM, e devem evocar diagnósticos alternativos (tais como sarcoidose, anomalia do desenvolvimento venoso, telangiectasia capilar);
- Lesões que realçam em T1 são definidas como áreas de hipersinal de pelo menos 3 mm após ao menos 5 minutos da injeção do contraste, mais bem vistas em T1-Gd SE ou GRE, mais difíceis de serem observadas em MPRAGE ou PSIR. Idealmente, a ausência de realce deve ser confirmada em uma sequência T1 pré-contraste e deve haver uma lesão correspondente em T2/FLAIR (se ausente, mais provavelmente representa artefato de estruturas vasculares ou telangiectasia capilar).
- Os padrões de realce podem variar entre nodular, periférico completo ou incompleto (realce incompleto geralmente está presente em lesões maiores, periventriculares ou justacorticais). Realce leptomeníngeo em T1-Gd é raro e deve evocar diagnósticos alternativos (tais como neurossarcoidose e doenças granulomatosas). No entanto, realce leptomeníngeo focal pode estar presente em FLAIR-Gd, particularmente nos pacientes com formas progressivas de EM.
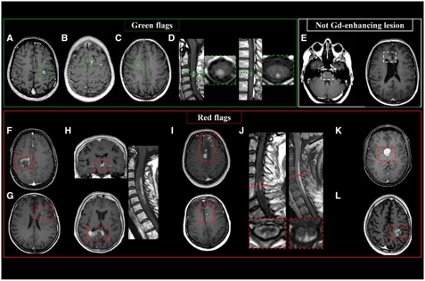
Figura 5 – Características das lesões de esclerose múltipla com gadolínio que são típicas, atípicas e aquelas que não devem ser incluídas.
– Em cima, à esquerda: exemplos de realce sugestivo de esclerose múltipla: (A) nodular; (B) anel aberto; (C) anel fechado; (D) realce nodular da medula espinhal.
– Em cima, à direita: (E) telangiectasia capilar (não deve ser contada para os critérios de diagnóstico).
– Linha inferior: (F) realce não homogêneo de uma grande (42 cm) lesão tumefativa, sugestiva de uma lesão inflamatória idiopática atípica desmielinizante; (G) realce em forma de banda na doença de Baló; (H) realce do diencéfalo, do corpo caloso (em um padrão “nuvem”), e uma lesão medular longitudinalmente extensa na NMO-SD; (I) realce leptomeníngeo, cortical e subcortical irregular em uma vasculite do SNC; (J) realce leptomeníngeo, pial e o ‘sinal do tridente’ na neurossarcoidose; (K) realce diencefálico homogêneo na encefalite anti-Ma2; (L) realce irregular e não homogêneo em glioblastoma.
Lesões dos nervos ópticos
Pontos-chave:
- Embora a avaliação dos nervos ópticos não seja necessária nos critérios atuais de diagnóstico de EM para demonstrar a disseminação no espaço, ela pode ser útil para confirmar o envolvimento destes e pode excluir diagnósticos alternativos para neuropatias ópticas atípicas;
- O protocolo ideal deve incluir sequências coronais T2 fat sat (com saturação de gordura) com resolução espacial submilimétrica (idealmente 0.5 x 0.5 mm ou melhores) e com espessura ≤ 3 mm, tipicamente 2D-STIR ou 2D-T2-FSE fat sat Para detecção de lesões agudas, uma sequência T1-Gd SE ou GRE fat sat é recomendada.
- Lesões típicas de EM têm hipersinal T2, efeito tumefativo e realce na fase aguda, geralmente unilaterais e anteriores. No entanto, estes achados não são específicos de EM, podendo ser encontrados em NMO-SD, lesões isquêmicas ou infecciosas. Lesões crônicas cursam com atrofia e hipersinal T2.
- Armadilhas incluem acometimento posterior / quiasmático (sugerindo NMO-SD anti-AQP4-IgG+), envolvimento bilateral e simultâneo de ambos os nervos ópticos e lesões longas, sugestivas de NMO-SD e, especialmente, sd. anti-MOG.
- Realce meníngeo das bainhas dos nervos ópticos pode ser visto na EM; no entanto, extensão às partes moles orbitárias ou seios cavernosos sinalizam outras etiologias (doenças granulomatosas, tumores, infecção, sd. anti-MOG).
Áreas de pesquisa em andamento
– Sinal da veia central: as lesões da EM tipicamente distribuem-se ao redor de veias e vênulas (detectável em ~80% das lesões), aspecto mais bem visualizado em alto campo magnético (7T), porém já visível em 3T e 1.5T, especialmente em sequências 3DT2*/SWI e em lesões da SB. A administração de Gd antes da aquisição aumenta a sensibilidade deste sinal, especialmente em 1.5T, não sendo necessária em ≥ 3T.
Ainda são necessários ensaios multicêntricos grandes e prospectivos, incluindo pacientes na apresentação inicial dos sinais neurológicos, para avaliar o valor clínico do sinal da veia central para o diagnóstico de esclerose múltipla.
– Desmielinização subpial: na EM, a desmielinização subpial é por vezes associada a inflamação meníngea e um LCR de perfil inflamatório. Este tipo de lesão parece ser altamente específico, porém ainda é subdetectado nos exames de RM mesmo com técnicas avançadas em magnetos de 1.5 e 3T. Ainda não foi estabelecida uma padronização com diretrizes atualizadas para a identificação deste tipo de lesão cortical.
– Lesões lentamente progressivas: estudos patológicos demonstram que até 57% das lesões da EM são ativas ou mistas. Tais lesões podem ser caracterizadas por aumento lento e progressivo do tamanho e da perda tecidual, mais comuns em doenças de longa duração, tipicamente com margem rica em ferro, micróglia e macrófagos atípicos. Tais lesões foram demonstradas in vivo em sequências de suscetibilidade magnética com halo periférico de hipossinal, que pode persistir por anos ou desaparecer gradualmente. Curiosamente, embora sejam comuns na EM, lesões deste tipo não são encontradas na NMO-SD ou em doenças cerebrovasculares. Embora a avaliação do “sinal do halo” seja promissora, até o momento, no entanto, não há consenso sobre o uso da melhor técnica para uso in vivo.
Conclusões
Lesões focais em hipersinal T2 são marcadores da EM, e a RM está formalmente incluída na investigação diagnóstica de pacientes com suspeita desta doença. Os critérios atuais por RM na EM são baseados em achados de imagem característicos, porém não suficientemente específicos.
Revisões sucessivas dos critérios diagnósticos aumentaram a sensibilidade da confirmação diagnóstica na apresentação inicial. No entanto, pouca atenção foi dada aos detalhes dos aspectos de imagem destes critérios, o que causa um risco de confusão diagnóstica em pacientes com poucas lesões e/ou comorbidades. Os guidelines propostos neste artigo têm a intenção de minimizar o risco de interpretações errôneas e aumentar a conscientização em relação aos diagnósticos diferenciais, sempre devendo ser utilizados no contexto de manifestações clínicas típicas da EM.
Desde que o exame seja feito em magneto de 1.5T ou superior e com protocolo adequado, os critérios de disseminação no tempo e no espaço e o monitoramento destes pacientes poderão ser feitos adequadamente.
Em situações desafiadoras, como em pacientes com poucas lesões ou comorbidades, tanto as características específicas de cada lesão quanto o padrão geral de todas as lesões devem ser considerados para diferenciar a EM de outras condições.
Sequências avançadas de RM têm demonstrado valor na distinção mais precisa de achados-chave e contribuirão para o aperfeiçoamento dos critérios diagnósticos no futuro.